Имаглив® (Imagliv®)
1-Z А Б В Г Д Е - Ж - З И - Й К Л М Н О П Р С Т У Ф Х Ц Ч - Щ Э Ю - Я
Клинико-фармакологическая форма - иматиниб
Форма выпуска
Таблетки, покрытые пленочной оболочкой 100 мг, 400 мг.
Описание препарата Имаглив® (Imagliv®)
Дозировка 100 мг: круглые, двояковыпуклые со скошенными краями таблетки, покрытые пленочной оболочкой от темно-желтого до оранжевокоричневого цвета, с гравировкой "NVR" на одной стороне и "SA" на другой стороне с риской между буквами "S" и "А".
Дозировка 400 мг: овальные, двояковыпуклые со скошенными краями таблетки, покрытые пленочной оболочкой от темно-желтого до оранжевокоричневого цвета, с гравировкой "400" на одной стороне и с риской между "SL" и "SL" на другой стороне.
Состав
1 таблетка, покрытая пленочной оболочкой, содержит:
действующее вещество: иматиниб 100 мг или 400 мг (эквивалентно 119,50 мг или 478,00 мг иматиниба мезилата);
вспомогательные вещества: целлюлоза микрокристаллическая 34,85 мг/ 139,40 мг, кросповидон 28,00 мг/ 112,00 мг, гипромеллоза 2,50 мг/ 10,00 мг, кремния диоксид коллоидный 1,25 мг/ 5,00 мг, магния стеарат 1,40 мг/ 5,60 мг;
оболочка: основная оболочкообразующая смесь желтая 8,55 мг/ 21,375 мг, основная оболочкообразующая смесь красная 0,45 мг/ 1,125 мг;
оболочкообразующая желтая смесь содержит: краситель железа оксид желтый (C.I. No. 77492, Е 172) 14,30 %, макрогол - 4000 7,15 %, тальк 7,15 %, гипромеллозу 71,40 %; оболочкообразующая красная смесь содержит: краситель железа оксид красный (C.I. No. 77491, Е 172) 14,30 %, макрогол - 4000 7,15 %, тальк 7,15 %, гипромеллозу 71,40 %.
Показания к применению
1. впервые выявленный положительный по филадельфийской хромосоме хронический миелоидный лейкоз (Ph+ХМЛ) у детей и взрослых;
2. Ph+ХМЛ в хронической фазе при неудаче предшествующей терапии интерфероном альфа или в фазе акселерации, или бластного криза у детей и взрослых;
3. впервые выявленный положительный по филадельфийской хромосоме (Ph+) острый лимфобластный лейкоз (ОЛЛ) у взрослых пациентов в комбинации с химиотерапией;
4. рецидивирующий или рефрактерный Ph+ОЛЛ у взрослых пациентов в качестве монотерапии;
5. миелодиспластические/миелопролиферативные заболевания, связанные с генными перестройками рецептора фактора роста тромбоцитов, у взрослых пациентов;
6. системный мастоцитоз у взрослых пациентов с отсутствием D816V c-Kit мутации или с неизвестным c-Kit мутационным статусом;
7. гиперэозинофильный синдром (ГЭС) и/или хронический эозинофильный лейкоз у взрослых с позитивной или негативной аномальной FIP1L1-PDGFR альфа-тирозинкиназой;
8. неоперабельная, рецидивирующая и/или метастатическая выбухающая дерматофибросаркома у взрослых пациентов;
9. неоперабельные или метастатические злокачественные гастроинтестинальные стромальные опухоли (ГИСО), позитивные по с- Kit (CD117), у взрослых пациентов;
10. адъювантная терапия c-Kit+ (CD117) ГИСО у взрослых пациентов.
Противопоказания к применению
1. повышенная чувствительность к иматинибу или любому другому компоненту препарата;
2. беременность и период грудного вскармливания;
3. детский возраст до 2-х лет (эффективность и безопасность препарата у детей этого возраста до настоящего времени не установлены).
Возможные побочные эффекты
ВНИМАНИЕ! Если вы подозреваете, что при приеме препарата ваше самочувствие ухудшилось, появились какие-то побочные эффекты, нужно сразу же обратиться очно к врачу, назначившему препарат!
Профиль безопасности препарата Имаглив® хорошо изучен. Большинство пациентов при применении препарата испытывают те или иные нежелательные явления (НЯ). Наиболее частыми НЯ (>10 %), связанными с приемом препарата, были: нейтропения, тромбоцитопения, анемия, головная боль, диспепсия, отеки, увеличение массы тела, тошнота, рвота, диарея, миалгии, мышечные судороги, сыпь, слабость, боль в животе. В основном эти НЯ были легкими или умеренно выраженными, только 2-5 % пациентов прекращали терапию препаратом Имаглив® из-за развития НЯ.
Миелосупрессия, НЯ со стороны желудочно-кишечного тракта (ЖКТ), отеки и сыпь возникают при применении иматиниба как при ХМЛ, так и при ГИСО. У пациентов с ХМЛ чаще развивается миелосупрессия, а у пациентов с ГИСО - желудочно-кишечные и внутриопухолевые кровотечения, другие нарушения со стороны ЖКТ, такие как кишечная непроходимость, перфорация и изъязвление слизистой оболочки. Другими серьезными НЯ при применении иматиниба являются гепатотоксичность, острая почечная недостаточность, гипофосфатемия, нарушения со стороны дыхательной системы, синдром лизиса опухоли и задержка роста у детей.
Часто отмечались периферические отеки преимущественно в периорбитальной области и нижних конечностях.
Типы НЯ и частота их развития схожи при приеме иматиниба взрослыми и детьми с лейкозами. Сочетанные побочные эффекты, такие как плевральный выпот, асцит, отек легких и быстрое увеличение массы тела (с периферическими отеками или без них), которые могут быть классифицированы как "задержка жидкости", в некоторых случаях способны достигать степени серьезных (в том числе жизнеугрожающих).
Возможна коррекция дозы препарата в зависимости от степени выраженности НЯ, вплоть до отмены препарата.
В соответствии с рекомендациями Всемирной организации здравоохранения (ВОЗ) нежелательные эффекты классифицированы в соответствии с частотой их развития следующим образом: очень часто (?1/10), часто (от ?1/100 до <1/10), нечасто (от ?1/1000 до <1/100), редко (от ?1/10000 до <1/1000), очень редко (<1/10000); частота неизвестна - по имеющимся данным установить частоту возникновения не представлялось возможным.
Инфекционные и паразитарные заболевания
нечасто: герпес простой, герпес опоясывающий, назофарингит, пневмония1, синусит, воспаление подкожной клетчатки, инфекции верхних дыхательных путей (в т.ч. грипп), инфекции мочевыводящих путей, гастроэнтерит, сепсис;редко:
микозы.Нарушения со стороны крови и лимфатической системы
очень часто:
нейтропения, тромбоцитопения, анемия;часто:
панцитопения, фебрильная нейтропения;нечасто:
тромбоцитемия, лимфопения, выраженное угнетение костномозгового кроветворения, эозинофилия, лимфаденопатия;редко:
гемолитическая анемия.Нарушения со стороны обмена веществ и питания
часто:
анорексия;нечасто:
гипокалиемия, повышение или снижение аппетита, гипофосфатемия, дегидратация, гиперурикемия, подагра, гиперкальциемия, гипергликемия, гипонатриемия;редко:
гиперкалиемия, гипомагниемия.Нарушения со стороны нервной системы
очень часто:
головная боль2;часто:
бессонница, головокружение, парестезии, нарушение вкуса, гипестезии;нечасто:
депрессия, тревога, снижение либидо, мигрень, сонливость, обморок, периферическая нейропатия, нарушения памяти, ишиас, синдром "беспокойных" ног, тремор, геморрагический инсульт;редко:
спутанность сознания, повышение внутричерепного давления, судороги, неврит зрительного нерва.Нарушения со стороны органа зрения
часто: отек век, повышение слезоотделения, конъюнктивальные кровоизлияния, конъюнктивит, синдром "сухого глаза", нечеткость (затуманенность) зрения;
нечасто: раздражение глаз, боль в глазах, орбитальный отек, кровоизлияния в склеру глаза, кровоизлияния в сетчатку, блефарит, макулярный отек;редко:
катаракта, отек диска зрительного нерва, глаукома.Нарушения со стороны органа слуха и лабиринтные нарушения
нечасто:
вертиго (головокружение), шум в ушах, снижение слуха.Нарушения со стороны сердечно-сосудистой системы
часто:
"приливы"3, кровоизлияния;нечасто:
ощущение сердцебиения, хроническая сердечная недостаточность4, отек легких, тахикардия, повышение или снижение артериального давления, гематомы (в т.ч. субдуральные гематомы), похолодание конечностей, синдром Рейно;редко:
аритмии (в т.ч. фибрилляция предсердий, внезапная остановка сердца), инфаркт миокарда, стенокардия, перикардиальный выпот.Нарушения со стороны дыхательной системы
, органов грудной клетки, средостениячасто:
носовое кровотечение, одышка, кашель;нечасто:
плевральный выпот5, боли в глотке или гортани, фарингит;редко:
плевральная боль, легочный фиброз, легочная гипертензия, легочные кровоизлияния.Нарушения со стороны желудочно-кишечного тракта
очень часто:
тошнота, рвота, диарея, диспепсия, боли в животе6;часто:
вздутие живота, метеоризм, запор, гастро-эзофагеальный рефлюкс, сухость во рту, гастрит;нечасто:
стоматит, изъязвление слизистой оболочки полости рта, желудочно-кишечные кровотечения7, отрыжка, мелена, эзофагит, асцит, изъязвление слизистой оболочки желудка, рвота кровью, хейлит, дисфагия, панкреатит;редко:
колит, паралитическая/обтурационная кишечная непроходимость, воспалительные заболевания кишечника.Нарушения со стороны печени и
желчевыводящих путейчасто:
повышение активности "печеночных" трансаминаз;нечасто:
желтуха, гепатит, гипербилирубинемия;редко:
печеночная недостаточность, некроз печени8.Нарушения со стороны кожи и подкожных тканей
очень часто:
периорбитальные отеки, дерматит, экзема, кожная сыпь;часто:
отечность лица, зуд, сухость кожи, эритема, алопеция, ночная потливость, реакции фотосенсибилизации;нечасто:
пустулезная сыпь, петехии, повышенное потоотделение, крапивница, экхимозы, повышенная предрасположенность к образованию гематом, гипотрихоз, гиперпигментация/гипопигментация кожи, эксфолиативный дерматит, повреждение ногтей, фолликулит, псориаз, пурпура, буллезная сыпь;редко:
острый фебрильный нейтрофильный дерматоз (синдром Свита), изменение цвета ногтей, ангионевротический отек, мультиформная эритема (в т.ч. синдром Стивенса-Джонсона), везикулярная сыпь, лейкокластический васкулит, острая генерализованная пустулезная экзантема.Нарушения со стороны скелетно-мышечной и соединительной ткани
очень часто:
мышечные спазмы и судороги, костно-мышечные боли (миалгии, артралгии, боль в костях9);часто:
припухлость суставов;нечасто:
скованность мышц и суставов;редко:
мышечная слабость, артрит.Нарушения со стороны почек и мочевыводящих путей
нечасто:
боль в области почек, гематурия, острая почечная недостаточность, учащенное мочеиспускание.Нарушения со стороны половых органов и молочных желез
нечасто:
гинекомастия, эректильная дисфункция, меноррагия, нарушения менструального цикла, сексуальная дисфункция, боль в сосках, увеличение молочных желез, отек мошонки.Общие расстройства и нарушения в месте введения
очень часто:
задержка жидкости и отеки, повышенная утомляемость, увеличение массы тела;часто:
слабость, повышение температуры тела, анасарка, озноб, дрожь, снижение массы тела;нечасто:
боль в груди, общее недомогание.Лабораторные и инструментальные данные
нечасто:
повышение активности щелочной фосфатазы, креатинфосфокиназы, лактатдегидрогеназы и содержания креатинина в плазме крови;редко:
повышение активности амилазы в плазме крови.1 Пневмония наиболее часто отмечалась у пациентов с ХМЛ в фазе акселерации, бластного криза и с неоперабельными и/или метастатическими ГИСО.
2 Головная боль наиболее часто отмечалась у пациентов с неоперабельными и/или метастатическими ГИСО.
3 "Приливы" наиболее часто отмечалась у пациентов с неоперабельными и/или метастатическими ГИСО; кровотечения (гематомы, геморрагии) наиболее часто отмечалась у пациентов с ХМЛ в фазе акселерации, бластного криза и с неоперабельными и/или метастатическими ГИСО.
4 Нежелательные явления со стороны сердца, включая хроническую сердечную недостаточность, чаще отмечались у пациентов с ХМЛ в фазе акселерации и при бластном кризе по сравнению с пациентами с ХМЛ в хронической фазе (длительность наблюдения 1 год).
5 Плевральный выпот чаще отмечался у пациентов с ХМЛ в фазе акселерации и при бластном кризе по сравнению с пациентами с ХМЛ в хронической фазе (длительность наблюдения 1 год).
6/7 Боль в животе и желудочно-кишечные кровотечения наиболее часто отмечались у пациентов с неоперабельными и/или метастатическими ГИСО.
8 Сообщалось об отдельных случаях развития печеночной недостаточности и некроза печени.
9 Мышечно-скелетные боли, включая миалгии, артралгии, боль в костях, чаще отмечались у пациентов с ХМЛ по сравнению с пациентами с неоперабельными и/или метастатическими ГИСО.
Пострегистрационный опыт применения
В ходе применения препарата Имаглив® также отмечались следующие побочные действия (их связь между применением препарата и нижеперечисленными НЯ не установлена, размер популяции пациентов неизвестен):
Нарушения со стороны нервной системы
нечасто: отек мозга.Нарушения со стороны органа зрения
редко:
кровоизлияния в стекловидное тело.Нарушения со стороны сердечнососудистой системы
нечасто:
тромбозы/эмболии;редко:
перикардит, тампонада сердца;очень редко:
анафилактический шок.Нарушения со стороны дыхательной системы, органов грудной клетки
, средостениянечасто:
острая дыхательная недостаточность1, интерстициальная болезнь легких.Нарушения со стороны желудочно-кишечного тракта
нечасто:
паралитическая/обтурационная кишечная непроходимость, кровотечения из опухоли ЖКТ, некроз опухоли ЖКТ, перфорация ЖКТ2;редко:
дивертикулит, сосудистая эктазия антрального отдела желудка (GAVE-синдром)3Нарушения со стороны кожи и подкожных тканей
нечасто:
ладонно-подошвенная эритродизестезия;редко:
лихеноидный кератоз, красный плоский лишай;очень редко:
токсический эпидермальный некролиз;частота неизвестна:
лекарственная сыпь с эозинофилией и системными симптомами.Нарушения со стороны скелетно-мышечной и соединительной ткани
редко:
аваскулярный некроз/некроз головки бедренной кости, рабдомиолиз/миопатия; частота неизвестна: задержка роста у детей.Нарушения со стороны половых органов и молочной железы
очень редко:
кровотечение из желтого тела/кисты яичника.Доброкачественные
, злокачественные и неуточненные новообразования (включая кисты и полипы)редко:
синдром лизиса опухоли.1 Имеются отдельные сообщения о развитии выраженной острой дыхательной недостаточности с летальным исходом у пациентов с тяжелыми инфекционными заболеваниями, выраженной нейтропенией и другими серьезными сопутствующими заболеваниями.
2 Сообщалось об отдельных случаях развития перфораций ЖКТ с летальным исходом.
3 В пострегистрационном периоде получены отдельные сообщения о случаях сосудистой эктазии антрального отдела желудка (GAVE-синдром).
Если любые из указанных в инструкции побочных эффектов усугубляются, или Вы заметили любые другие побочные эффекты, не указанные в инструкции, сообщите об этом врачу.
Дозировка, как принимать Имаглив® (Imagliv®)
Препарат следует принимать внутрь, во время еды, запивая полным стаканом воды (для снижения риска развития желудочно-кишечных расстройств).
Дозы 400 и 600 мг в сутки принимают за 1 прием; суточную дозу 800 мг следует разделить на 2 приема - по 400 мг утром и вечером.
Пациентам, не имеющим возможности проглотить таблетку целиком, например детям, препарат можно принимать в разведенном виде, для чего таблетки разводят водой или яблочным соком.
Необходимое количество таблеток помещают в стакан, заливают жидкостью (приблизительно 50 мл жидкости для таблетки 100 мг и 100 мл - для таблетки 400 мг) и размешивают ложкой, в результате чего образуется суспензия. Получившуюся суспензию следует принимать внутрь сразу после приготовления.
Лечение препаратом проводят до тех пор, пока сохраняется клинический эффект.
При ХМЛ рекомендуемая доза препарата Имаглив® зависит от фазы заболевания. В хроническую фазу ХМЛ доза составляет 400 мг/сут; в фазу акселерации и при бластном кризе - 600 мг/сут.
В случае прогрессирования ХМЛ (на любой стадии), при отсутствии удовлетворительного ответа на терапию (отсутствие полного гематологического ответа после 3 месяцев лечения, цитогенетического - через 12 месяцев терапии или при утрате ранее достигнутого ответа), если отсутствуют выраженные побочные эффекты и нейтропения/тромбоцитопения, не связанные с лейкозом, возможно повышение дозы с 400 мг до 600 мг или до 800 мг в сутки у пациентов в хронической фазе заболевания, и с 600 мг до 800 мг в сутки у пациентов в фазе акселерации и при бластном кризе.
Расчет режима дозирования у детей старше 2-х лет основывается на площади поверхности тела. Доза 340 мг/м2 в сутки рекомендуется у детей с хронической фазой ХМЛ и фазой акселерации. Общая суточная доза у детей не должна превышать 600 мг. Суточную дозу препарата можно принимать одномоментно или разделить на 2 равных приема - утром и вечером.
При Ph+ ОЛЛ у взрослых рекомендуемая доза препарата Имаглив® составляет 600 мг в сутки.
При миелодиспластических/миелопролиферативных заболеваниях у взрослых рекомендуемая доза препарата Имаглив® составляет 400 мг в сутки.
При применении препарата в качестве адъювантной терапии у пациентов с гастроинтестинальными стромальными опухолями рекомендуемая доза составляет - 400 мг/сут. Минимальная продолжительность лечения 3 года. Оптимальная длительность адъювантной терапии не установлена.
При неоперабельных и/или метастатических злокачественных ГИСО рекомендуемая доза препарата Имаглив® составляет 400 мг в сутки. При отсутствии побочных эффектов препарата и недостаточном ответе возможно увеличение суточной дозы препарата Имаглив® с 400 мг до 600 мг или до 800 мг.
При появлении признаков прогрессирования заболевания терапию препаратом Имаглив®следует прекратить.
При неоперабельной, рецидивирующей и/или метастатической выбухающей дерматофибросаркоме рекомендуемая доза препарата Имаглив® составляет 800 мг в сутки.
При системном мастоцитозе при отсутствии D816V c-Kit мутации или неизвестном мутационном статусе или недостаточной эффективности предшествующей терапии рекомендуемая доза препарата Имаглив® у взрослых составляет 400 мг в сутки.
При системном мастоцитозе, обусловленном аномальной FIP1L1-PDGFR ?-тирозинкиназой, образующейся в результате слияния генов Fip like 1 и PDGFR, рекомендуемая начальная доза составляет 100 мг в сутки. При недостаточной эффективности и отсутствии выраженных побочных эффектов возможно повышение дозы до 400 мг/сут.
При ГЭС и/или хроническом эозинофильном лейкозе (ХЭЛ) у взрослых рекомендуемая доза составляет 400 мг/сут. У пациентов с ГЭС/ХЭЛ, обусловленных аномальной FIP1L1-PDGFR ?-тирозинкиназой, рекомендуемая начальная доза составляет 100 мг в сутки. При недостаточной эффективности и отсутствии выраженных побочных эффектов возможно повышение дозы до 400 мг/сут.
При рецидивирующем или рефрактерном Ph+ ОЛЛ у взрослых пациентов рекомендованная доза составляет 600 мг/сут.
Пациенты с нарушением функции печени
Поскольку иматиниб метаболизируется главным образом в печени, пациентам с нарушениями функции печени препарат Имаглив®следует назначать в минимальной суточной дозе - 400 мг. При развитии выраженных нежелательных эффектов дозу препарата необходимо уменьшить. Следует с особой осторожностью назначать препарат пациентам с тяжелой печеночной недостаточностью.
Пациенты с нарушением функции почек
Почки не играют существенной роли в выведении иматиниба и его метаболитов. У пациентов с нарушениями функции почек или у пациентов, которым требуется систематическое проведение гемодиализа, лечение препаратом Имаглив® следует начинать с минимальной эффективной дозы - 400 мг 1 раз в сутки, соблюдая осторожность.
При непереносимости препарата Имаглив® начальная доза препарата может быть снижена, при недостаточной эффективности увеличена.
Пациенты пожилого возраста
У пациентов пожилого возраста не требуется коррекции режима дозирования препарата.
Коррекция режима дозирования при развитии негематологических побочных эффектов препарата
При развитии любого серьезного негематологического побочного эффекта, связанного с приемом препарата, терапию следует прервать до разрешения ситуации. Затем лечение может быть возобновлено с использованием дозы препарата, величина которой зависит от тяжести наблюдавшегося побочного эффекта. При увеличении концентрации билирубина и активности "печеночных" трансаминаз в сыворотке крови, соответственно, в 3 и 5 раз превышающих верхнюю границу нормы (ВГН), лечение препаратом следует временно приостановить до снижения концентрации билирубина до значения менее 1,5хВГН и активности "печеночных" трансаминаз до значений менее 2,5хВГН.
Терапию препаратом Имаглив® возобновляют с уменьшенной суточной дозы: у взрослых дозу уменьшают с 400 мг до 300 мг в сутки или с 600 мг до 400 мг в сутки, или с 800 мг до 600 мг в сутки; у детей - с 340 до 260 мг/м2 в сутки.
Коррекция режима дозирования при развитии серьезных побочных эффектов со стороны системы кроветворения (тяжелые тромбоцитопения, нейтропения).
При возникновении нейтропении и тромбоцитопении требуется временная отмена препарата или уменьшение его дозы в зависимости от степени выраженности этих нежелательных явлений.
При системном мастоцитозе (СМ) и ГЭС/ХЭЛ, обусловленных аномальной FIP1L1-PDGFR ?-тирозинкиназой (начальная доза препарата Имаглив®100 мг), в случае снижения абсолютного количества нейтрофилов в крови до уровня <1x109/л и/или количества тромбоцитов в крови до уровня <50x109/л рекомендуется отменить Имаглив® до тех пор, пока абсолютное число нейтрофилов не возрастет до ?1,5x109/л, а число тромбоцитов не увеличится до ?75x109/л, затем возобновить лечение препаратом Имаглив® в дозе, применявшейся до прерывания терапии.
При хронической фазе ХМЛ у детей и взрослых, ГИСО у взрослых пациентов, миелодиспластических/ миелопролиферативных заболеваниях, СМ и ГЭС/ХЭЛ у взрослых пациентов (начальная суточная доза для взрослых - 400 мг, для детей - 340 мг/м2) в случае снижения абсолютного количества нейтрофилов до уровня <1x109/л и/или количества тромбоцитов до уровня <50x109/л рекомендуется отменить Имаглив® до тех пор, пока абсолютное количество нейтрофилов не возрастет до ?1,5x109/л, а количество тромбоцитов не увеличится до ?75x109/л, затем возобновить лечение препаратом Имаглив® в дозе, применявшейся до прерывания терапии.
В случае повторного снижения количества нейтрофилов до уровня <1x109/л и/или количества тромбоцитов до уровня <50x109/л следует повторить вышеуказанные действия, а затем возобновить лечение препаратом Имаглив® в уменьшенной дозе 300 мг (у детей - 260 мг/м2).
В фазу акселерации и властного криза ХМЛ у детей и взрослых и при Рh+ ОЛЛ у взрослых пациентов (начальная суточная доза для взрослых - 600 мг, для детей - 340 мг/м2) в случае снижения абсолютного количества нейтрофилов до уровня <0,5x109/л и/или количества тромбоцитов до уровня <10x109/л после одного и более месяцев лечения рекомендуется:
1. проверить, является ли цитопения следствием лейкоза (исследование костного мозга);
2. если цитопения не связана с лейкозом, уменьшить дозу препарата Имаглив® до 400 мг (у детей - 260 мг/м2);
3. если цитопения сохраняется в течение 2 недель, уменьшить дозу до 300 мг (у детей - 200 мг/м2);
4. если цитопения сохраняется в течение 4 недель и ее связь с лейкозом не подтверждена, отменить иматиниб до тех пор, пока абсолютное количество нейтрофилов не станет ?1x109/л и тромбоцитов ?20x109/л; затем возобновить лечение препаратом Имаглив в дозе 300 мг (у детей - 200 мг/м2).
При неоперабельной, рецидивирующей и/или метастатической выбухающей дерматофибросаркоме (начальная доза препарата Имаглив® 800 мг) в случае снижения абсолютного количества нейтрофилов до уровня <1x109/л и/или количества тромбоцитов до уровня <50x109/л рекомендуется отменить Имаглив® до тех пор, пока абсолютное число нейтрофилов не возрастет до ?1,5x109/л, а количество тромбоцитов не увеличится до ?75x109/л, затем возобновить лечение препаратом Имаглив® в дозе 600 мг.
В случае повторного снижения количества нейтрофилов до уровня <1x109/л и/или количества тромбоцитов до уровня <50x109/л следует вышеуказанные повторить действия, а затем возобновить лечение препаратом Имаглив® в уменьшенной дозе 400 мг.
Влияние на беременность
Исследования на животных показали, что препарат обладает репродуктивной токсичностью. Имеются сообщения о случаях спонтанного прерывания беременности и увеличения частоты пороков развития плода. По этой причине иматиниб противопоказан по время беременности. Женщины репродуктивного возраста должны применять эффективные меры контрацепции в течение всего периода лечения препаратом и в течение трех месяцев после прекращения лечения.
Иматиниб и его активные метаболиты проникают в грудное молоко, при необходимости применения препарата в период грудного вскармливания, следует решить вопрос о прекращении грудного вскармливания.
Управление транспортом
Некоторые побочные эффекты препарата, такие как головокружение и нечеткость зрения, могут отрицательно влиять на способность к управлению автотранспортом и к выполнению потенциально опасных видов деятельности, требующих повышенной концентрации внимания и быстроты психомоторных реакций. При возникновении вышеперечисленных нежелательных явлений следует воздержаться от выполнения указанных видов деятельности.
Дополнительные указания при приеме Имаглив®
Лечение препаратом Имаглив® следует проводить только под наблюдением врача, имеющего опыт работы с противоопухолевыми препаратами.
При обращении с препаратом следует избегать попадания его на кожу и в глаза, а также вдыхания порошка препарата.
Опыт лечения препаратом Имаглив® ХМЛ у детей младше 2-х лет и Ph+ ОЛЛ у детей младше 1 года ограничен. Долгосрочные эффекты длительного воздействия препарата Имаглив® на рост у детей неизвестны, однако, так как имеются сообщения о случаях задержки роста, рекомендуется проводить тщательный контроль роста у детей, получающих препарат Имаглив®. Рекомендуется соблюдать осторожность при одновременном применении препарата Имаглив® и препаратов, которые являются субстратами изофермента CYP3A4 и имеют узкий терапевтический диапазон (см. Раздел "Взаимодействие с другими лекарственными средствами").
Угнетение кроветворения
Частота угнетения кроветворения и степень его выраженности зависят от стадии ХМЛ и используемой дозы препарата, они максимальны в случае применения препарата в высоких дозах. Угнетение кроветворения на фоне применения препарата Имаглив® у пациентов с ХМЛ обратимо и в большинстве случаев не требует отмены препарата или уменьшения его дозы. Также отмечаются случаи лимфопении. При использовании препарата Имаглив® рекомендуется регулярно осуществлять контроль клеточного состава крови и функции печени (активность "печеночных" трансаминаз и щелочной фосфатазы, концентрация билирубина).
Отеки и задержка жидкости
Отеки являются частым побочным эффектом терапии иматинибом. Частота возникновения отеков у пациентов, получающих иматиниб по всем показаниям, составляет более 50%. Частота и степень их выраженности, по-видимому, коррелирует с концентрацией препарата в плазме крови. Выраженная задержка жидкости (накопление ее в плевральной полости, отек легких, асцит и т.д.) наблюдается примерно у 2,5 % пациентов с ХМЛ. Чаще всего возникают периорбитальные отеки, с несколько меньшей частотой - отеки нижних конечностей. Специфического лечения обычно не требуется. Для своевременного выявления задержки жидкости рекомендуется регулярный контроль массы тела пациентов. В случае неожиданного быстрого увеличения массы тела, следует провести обследование пациента и, при необходимости, временно прекратить терапию препаратом Имаглив® и/или назначить диуретики. Наибольшая частота развития задержки жидкости отмечается у пожилых пациентов с сопутствующими сердечно-сосудистыми заболеваниями и почечной недостаточностью. Следует обеспечить тщательное наблюдение за пациентами с заболеваниями сердца, почечной недостаточностью или факторами риска их развития. У пациентов с поздними стадиями ХМЛ частота развития сердечной недостаточности была выше, чем у пациентов других категорий, что можно объяснить их ослабленным состоянием в целом. Большинство пациентов с отеками и задержкой жидкости являются лицами пожилого возраста (>65 лет).
В отдельных случаях выраженная задержка жидкости может иметь тяжелое течение с возможным летальным исходом. При применении препарата описан случай смерти пациента с ХМЛ в фазе бластного криза и комплексной симптоматикой: плевральным выпотом, развитием хронической сердечной и почечной недостаточности.
Гепатотоксичность
Препарат может оказывать токсическое действие на печень. Нарушения биохимических показателей функции печени, как правило, заключаются в незначительном повышении активности "печеночных" трансаминаз и повышении концентрации билирубина в сыворотке крови. Токсическое действие на печень обычно проявляется в течение первых двух месяцев лечения, однако, в ряде случаев, оно может проявляться и спустя 6-12 месяцев после начала лечения. Как правило, после отмены препарата биохимические показатели функции печени нормализуются в течение 1-4 недель. Выраженное повышение активности "печеночных" трансаминаз или билирубина отмечается менее чем у 3 % пациентов с ХМЛ и обычно проходит после снижения дозы препарата или кратковременного прерывания лечения (средняя продолжительность таких эпизодов в исследованиях составляла около 1 недели). При назначении препарата пациентам с заболеваниями печени следует регулярно оценивать клинический анализ крови и определять активность "печеночных" ферментов в плазме крови.
Кровоизлияние/кровотечение
Наиболее частыми клинически значимыми кровотечениями были кровотечения из ЖКТ. Чаще всего они возникали у пациентов с поздними стадиями ХМЛ и у пациентов с ГИСО, у которых они могут быть следствием основного заболевания (кровотечение из опухоли, обусловленное её некрозом). У пациентов с неоперабельными и/или метастатическими ГИСО в клинических исследованиях III фазы кровотечения различной локализации отмечались в 12,9 % случаев; в клинических исследованиях II фазы желудочно-кишечные кровотечения наблюдались у 8 пациентов (5,4 %), а кровотечения из опухолевых очагов - у 4 пациентов (2,7 %). Локализация кровотечений зависела от локализации опухолевых очагов. В пострегистрационном периоде получены отдельные сообщения о случаях сосудистой эктазии антрального отдела, зарегистрированных у пациентов с ХМЛ и ОЛЛ и другими заболеваниями. В случае необходимости следует рассмотреть возможность отмены терапии иматинибом. У пациентов с ХМЛ, у которых до начала лечения наблюдались признаки угнетения кроветворения, нередко отмечаются кровоизлияния в ЦНС или кровотечения из ЖКТ. Установлено, что у пациентов с лейкозами с острым развитием заболевания нередко возникают кровотечения/кровоизлияния, обусловленные тромбоцитопенией или тромбоцитопатией.
При начале и во время терапии иматинибом следует внимательно оценивать наличие симптомов со стороны ЖКТ.
Сыпь и тяжелые кожные нежелательные реакции
Кожная сыпь отмечается примерно у трети всех пациентов, получающих иматиниб по всем показаниям. Она часто сопровождается зудом и, как правило, проявляется в виде эритематозных, пятнисто-папулезных высыпаний на предплечьях, туловище или лице. Хотя в большинстве случаев сыпь легкая и проходит без лечения, в более тяжелых случаях может потребоваться временная или полная отмена препарата. Как правило, выраженность сыпи уменьшается после назначения антигистаминных препаратов и местных глюкокортикостероидов, однако, в некоторых случаях требуется их системное применение.
Кишечная непроходимость, перфорация или изъязвление слизистой оболочки желудка или кишечника
У небольшой части пациентов на фоне терапии иматинибом отмечается язвенное поражение ЖКТ, которое в отдельных случаях может быть следствием местного раздражающего действия иматиниба. Геморрагический некроз опухоли и перфорация ЖКТ наиболее часто наблюдаются у пациентов с ГИСО. В случае метастазирующих ГИСО некроз опухоли может возникать на фоне лечебного патоморфоза, что в редких случаях приводит к перфорации. Непроходимость ЖКТ также чаще возникает у пациентов с ГИСО, ее причиной могут быть метастазы или спайки, возникшие в результате ранее проведенного оперативного лечения.
Гипотиреоз
На фоне применения препарата Имаглив® у пациентов, перенесших тиреоидэктомию и получающих заместительную терапию левотироксином натрия, могут отмечаться случаи развития гипотиреоза. Необходимо регулярно проводить определение концентрации тиреотропного гормона у данной категории пациентов.
Гиперэозинофильный синдром
У пациентов с ГЭС и заболеваниями сердца (либо скрытой инфильтрацией миокарда ГЭС-клетками) в начале терапии иматинибом отмечались отдельные случаи развития кардиогенного шока/левожелудочковой недостаточности. Эти нежелательные явления купируются введением системных глюкокортикостероидов, принятием мер, направленных на поддержание кровообращения, временной отменой препарата Имаглив®.
У пациентов с МДС/МПЗ и высоким числом эозинофилов следует контролировать функцию сердца (ЭКГ и определение сывороточной концентрации кардиоспецифичного тропонина). При выявлении отклонений от нормы в начале терапии следует рассмотреть возможность профилактического применения системных глюкокортикостероидов (1-2 мг/кг) в течение 1-2 недель одновременно с иматинибом.
Синдром лизиса опухоли
Вследствие риска развития синдрома лизиса опухоли, перед назначением препарата Имаглив® следует обеспечить адекватную гидратацию организма пациента и контролировать уровень мочевой кислоты до начала и во время лечения.
Репродуктивный возраст
Женщинам репродуктивного возраста во время терапии препаратом Имаглив® и как минимум в течение трех месяцев после окончания лечения препаратом следует использовать надежные способы контрацепции.
Оценка эффекта терапии
Молекулярный мониторинг ответа на терапию препаратом Имаглив® у пациентов с Ph+ ХМЛ должен выполняться рутинно каждые 3 месяца до достижения большого молекулярного ответа, а затем не реже, чем каждые 6 месяцев. Проведение молекулярного мониторинга рекомендуется также при изменениях в проводимой терапии. Молекулярный мониторинг позволяет оценить эффективность терапии ингибиторами тирозинкиназ (ИТК) у пациентов с ХМЛ, в том числе недостаточный ответ на терапию или его утрату, например, вследствие сниженной приверженности пациента к лечению (прекращение приема препарата, нерегулярный прием), развития межлекарственных взаимодействий, развития резистентности к терапии. Полимеразная цепная реакция (ПЦР) в реальном времени - наиболее предпочтительный метод мониторинга, в связи с высокой его чувствительностью и малоинвазивным характером.
Пациенты, которым подобный мониторинг проводится каждые 3-4 месяца, имеют более высокий показатель безрецидивной выживаемости по сравнению с пациентами, которым такие исследования выполняются реже. В случае неудовлетворительного ответа на терапию при отсутствии факторов, снижающих ее эффективность (низкая приверженность пациента к лечению, межлекарственные взаимодействия), следует рассмотреть возможность изменения тактики лечения (например, назначение альтернативного препарата-ингибитора тирозинкиназ).Тяжелая печеночная недостаточность, тяжелые нарушения функции почек (включая пациентов, нуждающихся в регулярном проведении гемодиализа), пациенты с сердечно-сосудистыми заболеваниями и/или наличием факторов риска развития сердечной недостаточности, при одновременном применении с препаратами, ингибирующими изофермент CYP3A4, сильными индукторами изофермента CYP3A4, с препаратами, являющимися субстратами изофермента CYP3A4, парацетамолом, варфарином (см. раздел "Взаимодействие с другими лекарственными препаратами").
Передозировка
Опыт применения препарата Имаглив® в дозах, превышающих терапевтические, ограничен. В клинической практике отмечались единичные случаи передозировки препарата. В целом, исход таких случаев был благоприятным.
Антидот к препарату Имаглив® не известен. При передозировке рекомендуется медицинское наблюдение и проведение симптоматической терапии.
Передозировка у взрослых
При приеме препарата Имаглив® в дозе 1200-1600 мг/сут в течение 1-10 дней наблюдались тошнота, рвота, диарея, сыпь, эритема, отеки, местная припухлость, повышенная утомляемость, мышечные спазмы, тромбоцитопения, панцитопения, боль в животе, головная боль, снижение аппетита.
При приеме препарата в дозе 1800-3200 мг (наибольшая доза составляла 3200 мг в сутки в течение 6 дней) отмечались слабость, миалгия, повышение активности креатинфосфокиназы и концентрации билирубина, боли в животе. При однократном применении препарата Имаглив® в дозе 6400 мг у пациента развились тошнота, рвота, боль в животе, гипертермия, отек лица, снижение количества нейтрофилов и повышение активности "печеночных" трансаминаз в сыворотке крови.
При однократном приеме препарата в дозе 8-10 г отмечались рвота и боли в животе.
Передозировка у детей и подростков
При однократном приеме препарата в дозе 400 мг у трехлетнего ребенка отмечались рвота, диарея и анорексия.
При однократном приеме препарата Имаглив® в дозе 980 мг у ребенка в возрасте 3-х лет наблюдались снижение количества лейкоцитов в крови и диарея.
Как хранить препарат
В сухом месте при температуре не выше 30°С.
Препарат следует хранить в недоступном для детей месте.
Срок годности
3 года.
Препарат не следует использовать после истечения срока годности.
Условия отпуска
По рецептуИнформация по упаковке
Дозировка 100 мг: по 10 таблеток в блистер ПВХ/Ал. По 2 или 6 блистеров вместе с инструкцией по применению в картонную пачку.
Дозировка 400 мг: по 10 таблеток в блистер ПВХ/ПЭ/ПВДХ/Ал. По 1 или 3 блистера вместе с инструкцией по применению
Информация для врачей о препарате Имаглив®
Фармакологическая группа
Противоопухолевое средство - протеинтирозинкиназы ингибиторФармакодинамика
Иматиниб - ингибитор протеинтирозинкиназ, который оказывает мощное избирательное влияние на активность BCR-ABL тирозинкиназы (ТК), а так же на некоторые другие ТК: рецептор фактора роста тучных и стволовых клеток (SCFR или белковая тирозинкиназа KIT, CD 117), рецепторы домена дискоидина (DDR1 и DDR2), рецептор колониестимулирующего фактора (CSF-1R), тромбоцитарные рецепторы фактора роста (PDGFR-? и PDGFR-?). Иматиниб селективно подавляет пролиферацию и вызывает апоптоз клеточных линий, экспрессирующих BCR-ABL, включая незрелые лейкозные клетки, образующиеся у пациентов с положительными по филадельфийской хромосоме (Ph+) хроническим миелолейкозом (ХМЛ) и острым лимфобластным лейкозом (ОЛЛ). In vitro иматиниб селективно ингибирует BCR-ABL-позитивные колонии, полученные из клеток крови пациентов с ХМЛ.
Иматиниб ингибирует пролиферацию и индуцирует апоптоз клеток стромальных опухолей желудочно-кишечного тракта, экспрессирующих тирозинкиназу с мутацией c-Kit рецептора.
Активация рецепторов факторов роста тромбоцитов или ABL-фрагмента тирозинкиназы может являться причиной развития как миелодиспластических/миелопролиферативных заболеваний, так и гиперэозинофильного синдрома (ГЭС), хронического эозинофильного лейкоза и выбухающей дерматофибросаркомы. Активация c-Kit рецептора тирозинкиназы и рецепторов факторов роста тромбоцитов может лежать в основе патогенеза системного мастоцитоза. Иматиниб ингибирует передачу сигнала в клетках и клеточную пролиферацию, возникающие в результате нарушения регуляции активности факторов роста тромбоцитов и стволовых клеток, c-Kit-рецептора и ABL-фрагмента тирозинкиназы. При применении иматиниба у пациентов с неоперабельными и/или метастатическими злокачественными гастроинтестинальными стромальными опухолями (ГИСО) отмечается достоверное увеличение общей выживаемости пациентов (медиана выживаемости - 48,8 мес.) и выживаемости без признаков заболевания (21 мес.). Адъювантная терапия препаратом ГИСО снижает риск развития рецидивов на 89 %, увеличивает выживаемость без признаков заболевания (38 мес.). Адъювантная терапия иматинибом ГИСО в течение 1 года снижает риск развития рецидивов, увеличивает выживаемость без признаков заболевания. Адъювантная терапия препаратом ГИСО в течение 3 лет приводит к значительному увеличению общей выживаемости и выживаемости без признаков прогрессирования заболевания по сравнению с терапией в течение 1 года.
Фармакокинетика
Фармакокинетические параметры иматиниба оценивались при введении препарата в диапазоне доз от 25 мг до 1000 мг. Фармакокинетические профили анализировались в 1-й день, а также по достижению равновесных концентраций иматиниба в плазме крови на 7-й или 28-й день.
Всасывание
После приема внутрь биодоступность препарата составляет в среднем 98 %. Коэффициент вариации для показателя площадь под кривой "концентрация-время" (AUC) составляет 40-60 %. При введении иматиниба в диапазоне доз от 25 до 1000 мг отмечена прямая линейная зависимость AUC от величины дозы.
При приеме препарата с пищей с высоким содержанием жиров отмечается незначительное снижение степени всасывания (уменьшение максимальной концентрации иматиниба в плазме крови на 11 % и величины AUC на 7,4 %) и замедление скорости всасывания (увеличение времени достижения максимальной концентрации иматиниба в плазме крови на 1,5 ч) в сравнении с приемом натощак.
Распределение
Около 95 % иматиниба связывается с белками плазмы крови (главным образом с альбумином и кислым ?-гликопротеином, в незначительной степени - с липопротеинами).
Метаболизм
Иматиниб метаболизируется главным образом в печени с образованием основного метаболита (А-деметилированного пиперазинового производного), циркулирующего в кровяном русле. In vitro метаболит иматиниба обладает фармакологической активностью, сопоставимой с активностью исходного вещества. AUC метаболита составляет 16 % от AUC иматиниба. Связывание метаболита с белками плазмы подобно таковому для иматиниба.
Выведение
После однократного приема препарат выводится из организма в течение 7 дней, преимущественно в виде метаболитов (68 % - через кишечник и 13 % - почками). В неизмененном виде выводится около 25 % дозы (20 % - через кишечник и 5 % - почками). Период полувыведения иматиниба составляет около 18 ч.
При повторных приемах препарата 1 раз в сутки его фармакокинетические параметры существенно не изменяются, а равновесная концентрация иматиниба в плазме крови превышает исходную в 1,5-2,5 раза.
У пациентов старше 65 лет незначительно увеличивается объем распределения (на 12 %). Для пациентов с массой тела 50 кг средняя величина клиренса иматиниба составляет 8,5 л/ч, а для пациентов с массой тела 100 кг - 11,8 л/ч. Однако эти различия не являются существенными и не требуют коррекции дозы препарата в зависимости от массы тела пациента. Фармакокинетика иматиниба не зависит от пола. Изменения клиренса и объема распределения иматиниба при его одновременном применении с другими лекарственными средствами несущественны и не требуют изменения дозы препарата.
Дети и подростки: как и у взрослых пациентов, у детей и подростков младше 18 лет иматиниб при приеме внутрь быстро и практически полностью всасывается. Величины AUC у пациентов этой возрастной группы после приема иматиниба в дозах 260 и 340 мг/м2 сходны с таковыми у взрослых после приема препарата в дозах 400 мг и 600 мг, соответственно. При сравнении значений показателя AUC(0-24) У детей и подростков в 1-й и на восьмой дни при повторном приеме препарата в дозе 340 мг/м 1 раз в сутки отмечается возрастание величины этого показателя в 1,7 раз, свидетельствующее о кумуляции иматиниба. На основе объединенного популяционного фармакокинетического анализа у детей с гематологическими заболеваниями было показано, что клиренс иматиниба прямо пропорционален площади поверхности тела, другие демографические показатели (возраст, масса тела и индекс массы тела) не имеют клинически значимого влияния на экспозицию иматиниба.
Нарушение функции печени: у пациентов с нарушениями функции печени различной степени средние значения AUC не увеличиваются.
Нарушение функции почек: при применении иматиниба у пациентов с нарушениями функции почек легкой или средней степени (клиренс креатинина > 30 мл/мин) отмечается повышение экспозиции (воздействующего количества) препарата в плазме крови в 1,5-2,0 раза, соответствующее увеличению концентрации кислого ?-гликопротеина (основного белка плазмы, связывающегося с иматинибом). Поскольку только незначительное количество препарата выводится почками, клиренс свободного иматиниба был одинаковым у здоровых добровольцев и у пациентов с нарушениями функции почек. Корреляции между экспозицией препарата и тяжестью почечных нарушений не выявлено.
Взаимодействие с другими веществами
Препараты, которые могут снижать концентрацию иматиниба в плазме крови (совместное применение не рекомендуется)
Одновременное применение иматиниба с препаратами, являющимися индукторами изофермента CYP3A4 (рифампицин, дексаметазон, препараты из зверобоя продырявленного, противоэпилептические препараты: карбамазепин, окскарбазепин, фенитоин, фенобарбитал, фосфенитоин, примидон) может привести к ускорению метаболизма иматиниба и, как следствие, к снижению его концентрации в плазме крови. Согласно результатам исследований, концентрация иматиниба снижается на 54-74 %.
Препараты, которые могут повышать концентрацию иматиниба в плазме крови
При одновременном применении препарата иматиниба с препаратами, ингибирующими изофермент CYP3A4 цитохрома Р450 (например, ингибиторы протеазы (индинавир, лопинавир, ритонавир, саквинавир, телапревир, нелфинавир, боцепревир), позаконазол, вориконазол, телитромицин, кетоконазол, итраконазол, эритромицин, кларитромицин), возможно замедление метаболизма иматиниба и увеличение его концентрации в плазме крови (Сmах увеличивается на 26 %, AUC - на 40 %). Необходимо соблюдать осторожность при необходимости совместного назначения комбинаций иматиниба с этими препаратами или другими ингибиторами CYP3A4.
Препараты, концентрация которых может изменяться при назначении иматиниба
Иматиниб способен ингибировать некоторые изоферменты цитохрома Р450. При совместном назначении иматиниба и симвастатина Сmах и AUC симвастатина увеличивается в 2 и 3,5 раза соответственно, что обусловлено ингибированием CYP3A4 иматинибом.
Иматиниб способен увеличивать концентрации других препаратов, метаболизирующихся изоферментом CYP3A4 (триазолобензодиазепины, дигидропиридиновые блокаторы "медленных" кальциевых каналов (амлодипин, нефидипин и т.д.), большинство ингибиторов ГМГ-КоА-редуктазы (статинов).
Рекомендуется соблюдать особую осторожность при одновременном применении иматиниба и препаратов, которые являются субстратами изофермента CYP3A4 и имеют узкий терапевтический диапазон (например, такролимус, сиролимус, эрготамин, фентанил, терфенадин, бортезомиб, доцетаксел, хинидин, циклоспорин и пимозид). Иматиниб также ингибирует in vitro изоферменты CYP2C9 и CYP2C19.
При совместном применении иматиниба с варфарином наблюдалось удлинение протромбинового времени (ПВ). При одновременном применении с кумариновыми производными необходим краткосрочный мониторинг ПВ в начале и в конце терапии препаратом, а также при изменении режима дозирования иматиниба. В качестве альтернативы варфарину следует рассмотреть возможность использования низкомолекулярных гепаринов.
При комбинации иматиниба с химиотерапевтическими препаратами в высоких дозах возможно развитие транзиторной гепатотоксичности, проявляющейся повышением активности "печеночных" трансаминаз в сыворотке крови и гипербилирубинемией. Следует контролировать функцию печени при комбинации иматиниба и гепатотоксичных режимов химиотерапии.
In vitro иматиниб ингибирует изофермент CYP2D6 в тех же концентрациях, в которых он ингибирует изофермент CYP3 А4. При применении иматиниба в дозе 400 мг 2 раза в сутки вместе с метопрололом (субстратом изофермента CYP2D6), отмечается повышение Сmах и AUC метопролола приблизительно на 21 %, однако, учитывая несущественное усиление эффектов субстратов изофермента CYP2D6 при их совместном применении с иматинибом, изменения режима дозирования подобных препаратов не требуется.
In vitro иматиниб ингибирует О-глюкуронидацию парацетамола, в связи с чем необходимо соблюдать осторожность при одновременном применении иматиниба с парацетамолом (особенно при использовании высоких доз парацетамола).
У пациентов, перенесших тиреоидэктомию и получающих заместительную терапию левотироксином натрия, возможно снижение его плазменной концентрации при совместном использовании с иматинибом.
Недостаточно изучен вопрос лекарственного взаимодействия иматиниба и препаратов для химиотерапии у пациентов с Ph+ ОЛЛ.
Необходимо соблюдать осторожность при совместном использовании иматиниба и химиотерапевтических препаратов в связи с возможным повышением риска развития лекарственных осложнений, таких как гепатотоксичность и миелосупрессия и др.
Имеются сообщений о развитии поражения печени при совместном применении иматиниба и аспарагиназы.

Секреты долголетия: уроки из синих зон Земли

Влияние микропластика на здоровье: что говорят эксперты

Новый подход к менопаузе: заморозка ткани яичника может изменить все

Омега-3 vs. витамин D: что выбрать для здоровья иммунной системы?

Сможем ли мы добавить больше активной жизни к нашим годам?

Новое исследование: как фантазии помогают укрепить память
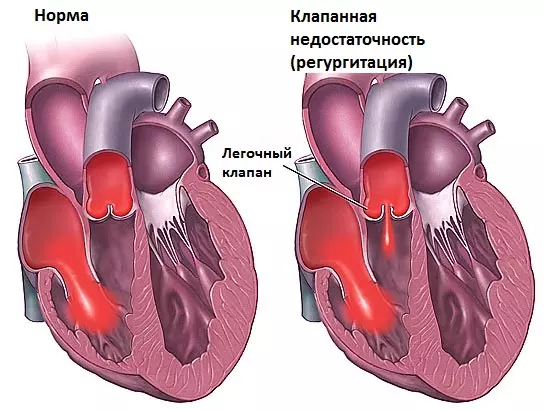 Недостаточность клапана легочной артерии
Недостаточность клапана легочной артерии Электрокардиографическая диагностика локализации критической окклюзии в коронарной артерии
Электрокардиографическая диагностика локализации критической окклюзии в коронарной артерии Контроль индивидуальной физической нагрузки на сердце
Контроль индивидуальной физической нагрузки на сердце Профилактика гипотонии, массаж, самомассаж, упражнения
Профилактика гипотонии, массаж, самомассаж, упражнения

